|
(记者方明诚/综合报导) 一家总部位于拉斯维加斯的公司生产了大部分在美国销售的堕胎药米非司酮(mifepristone),它日前向美国食品和药物管理局(FDA)提起诉讼,这是最近法院对该药物命运进行的一系列操控中最新一次的法律行动。
这起诉讼为德州联邦法院一起案件正在进行的激烈法律诉讼中又增加了一宗,在该案件中,一个反堕胎组织联盟正在寻求推翻 FDA 对米非司酮 23 年的批准,米非司酮是两种堕胎药丸流产方案的第一个。
在新案件中,生产米非司酮普及药的 GenBioPro 试图阻止 FDA 在法院一旦命令米非司酮退出市场时遵守规定。 该案件已提交至美国马里兰州地方法院。
本月早些时候,德州案件的联邦法官发布了一项初步裁决,宣布米非司酮的批准无效。 上周,联邦上诉法院的一个小组表示,在案件进行诉讼期间,该药物可能会留在市场上,但它下令撤销 FDA 自 2016 年以来对米非司酮采取的所有监管行动,其中包括 2019 年批准的完全相同药物的版本GenBioPro 。该命令已被最高法院暂时中止。
GenBioPro 的诉讼指称,一旦FDA 被勒令暂停或撤销其对 GenBioPro 产品的批准,FDA 就履次未能定规它将遵循国会制定的监管程序,并为制药公司提供宪法保障的正当程序。
诉讼称,FDA 保留了立即服从此类法院命令的可能性,“如果 GenBioPro 不停止米非司酮的运输,它就会面临严重的民事和刑事处罚风险。”
GenBioPro 首席执行官 Evan Masingill 表示,德州案件结果的不确定性导致米非司酮订单减少。“市场混乱已经无处不在,影响了包括数万个单位的订单,”他说。
此案还可能对更广泛的制药行业产生影响。 该诉讼称,FDA 遵循法院命令立即撤销对药物的批准将是史无前例的。 该诉讼称,只有当 FDA 确定该药物“对公众健康构成迫在眉睫的危害”时,该药物的批准才能被撤销。 FDA 在法庭上有力地辩称米非司酮非常安全,并引用了多项研究表明严重的并发症很少见,只有不到 1% 的患者需要住院治疗。
“人们在这个国家而不是在其他国家开发药物,因为我们通常有一个非常可预测的监管结构,而随着德克萨斯州的诉讼,情况是否会变成这样?” GenBioPro 的律师兼中左翼法律倡导组织 Democracy Forward 的总裁 Skye Perryman 说。 “这对整个行业都有影响。”
GenBioPro 表示,它供应了在美国销售的约三分之二的药物,并在 2017 年至 2020 年期间销售了超过 850,000 单位的药物。
GenBioPro 的诉讼引用了 FDA 提交给最高法院的文件,该机构在文件中表示,如果上诉法院的裁决生效,“该药物的普及制药(generic) 所获批准将完全停止。”该公司在诉讼中表示,此类声明相当于联邦机构的政策决定,“FDA 的决定是错误和非法的。”
FDA 专员 Robert Califf 博士日前在参议院拨款委员会作证时回答有关德州诉讼的问题时表示,该机构担心该案件的潜在影响“来自需要获得这种药物的患者的福祉, 制药业和我们执行法定权力的能力。”他指出 FDA 正在法庭上与此案抗争,并补充说,“我只想说 FDA 打算遵守任何法院命令。”
该诉讼称,FDA 拒绝对 GenB 提出的三封信作出回应。FDA 发表声明称,“FDA 不对未决诉讼发表评论。”
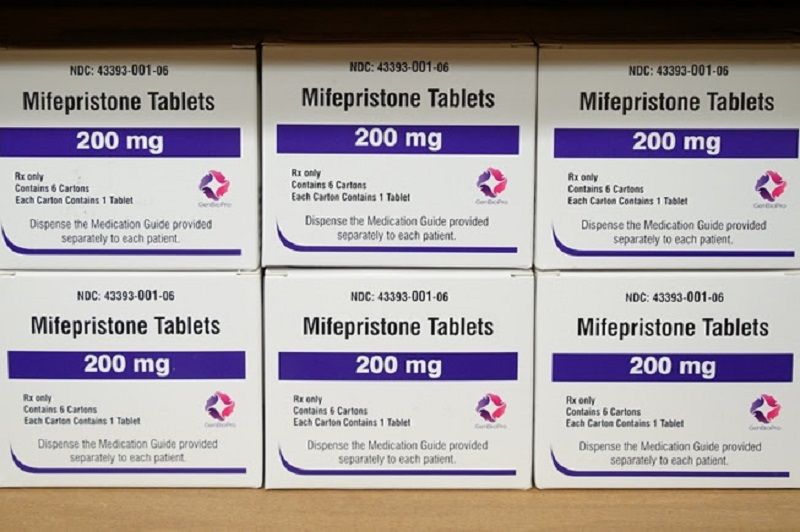
一拉斯维加斯公司是数十年合法堕胎药物米非司酮普及版的制药商。
|
